
遵医附院心血管内科石蓓教授团队在Nature旗下《Signal Transduction and Targeted Therapy》杂志(中科院1区Top, IF=39.3)发表最新成果
2023年11月20日,遵医附院心血管内科石蓓教授团队在Nature旗下的《Signal Transduction and Targeted Therapy》(中科院1区,IF=39.3分)杂志在线发表了题为“Hypoxia-induced signaling in the cardiovascular system: pathogenesis and therapeutic targets”的论文。该文系统性的总结了心血管疾病中缺氧的研究历史和重要里程碑事件,并详尽且辩证地探讨了心血管疾病中缺氧信号的多维度的调控通路及其机制,以及有关心血管疾病中缺氧信号的治疗靶点和临床研究进展。

遵义医科大学附属医院为本文的第一通讯单位,石蓓教授与遵医附院候鸟型学科带头人葛均波院士为本文的共同通讯作者。心血管内科赵永超副研究员(国家“博新计划”入选者、上海市“超级博士后”激励计划入选者、遵义医科大学“12345”未来人才培养计划之“科技菁英”计划入选者)为本文的第一作者,该工作得到了国家自然基金等多个项目的支持。
在进化过程中,随着多细胞的三维结构形成,它们需要以不同的方式自主适应不同的氧气水平。2019年,诺贝尔生理学或医学奖授予了美国医学家威廉・凯林(William G. Kaelin Jr.)、英国医学家彼得・拉特克利夫(Sir. Peter J. Ratcliffe)和美国医学家格雷格・塞门扎(Gregg L. Semenza),以表彰他们在动物细胞如何感知和适应氧气供应变化方面的重大发现。他们的研究阐明了生物体内氧气适应的关键机制,为理解氧气对细胞代谢和生理学的影响奠定了基础,也为治疗贫血、癌症和心血管问题等各种疾病提供了宝贵的见解和新的治疗途径。
心血管疾病占据了全球疾病负担的重要组成部分,而缺氧(即氧气供应不足的问题)与之密切相关。缺氧诱导因子(HIFs)作为生物体对缺氧的核心应答分子,在各个物种中表现出惊人的保守性。在心血管生物学领域,HIFs相关通路具有至关重要的地位。在发育的心脏中,孕期的缺氧事件激活了HIF-1控制的特定通路,对心脏心房和中隔的形成至关重要。在成年生物体内,一般来说,HIF-1α主要掌控缺氧的急性响应,包括激活糖酵解基因、降低氧气利用率和减少活性氧产生;而HIF-2α则调控缺氧的慢性代偿,包括促进红细胞生成、铁代谢、脂肪酸的合成和摄取、炎症反应、纤维化和血管生成。与此类似,心血管疾病既表现出急性事件的特征(如急性心梗),也伴随着慢性疾病的进展(如冠状动脉粥样硬化和心力衰竭等)。随着泛血管医学概念的兴起,研究HIFs与环境之间的相互作用变得越来越重要,尤其是在探讨其在心血管疾病中的共性和特殊性方面。
文中首次从时间和空间的维度整合了对“HIFs switch”的讨论,包括从缺氧的发生发展(氧气浓度的梯次下降)、缺氧的急慢性演替和缺氧的地理特征(高海拔的自然选择)等角度,体现了HIF-1α和HIF-2α的“互为主辅、相互交替”的作用特点(图1)。由于HIF-1α和HIF-2α结构的相似性,在缺氧条件下HIF-1/2α在心血管细胞中引起的共通性能量代谢改变决定了其反应的基础。但是鉴于HIF-1α和HIF-2α仍存在的不同特性,在相互联系、反馈的时空里,HIF-1α和HIF-2α在各自特定的时间和地点起着主导作用,这称之为“HIFs switch”。 具体到转录活性及其调控层面,经典地,在急性缺氧时,HIF-1α起主导作用,主要诱导血管新生。而在随后的慢性缺氧中,HIF-2α起主导作用,主要使得新生血管发育成熟和结构稳定(如平滑肌的招募等)。有趣的是,促红素(EPO)是最早被发现与HIF-1有关的。其对于遍布全身的红细胞和血红蛋白的合成有着至关重要的作用。然而近些年的研究表明,HIF-2对于EPO的合成似乎起着同等程度甚至更为重要的作用。红细胞作为血液中的携氧细胞,其功能和成分的改变对于心血管系统有着无法避免的影响。此外,肺脏通过血气交换首先感知外界氧含量的变化,而且由于直接接触空气,相对于其他器官是个富氧含量的器官。其HIFs反应系统也由此具备了特殊性。与肺脏相比,其他器官中的HIF-1α更容易在缺氧条件下激活。然而,在肺脏中,当氧浓度下降到6%时,HIF-2α会被优先激活,而此时HIF-1α的丰度增强并不明显。但总归而言,传统、经典的HIFs switch指的是在急慢性缺氧过程中HIF-1/2/3α异构体之间主导作用的顺次更替。而广义的HIFs switch则进一步地包含了在更长的时间维度下自然选择对于HIF-αs及其关联分子作用的平衡演替。由于高海拔处氧气在7%~21%之间,所以对于生活在低海拔地区的人群来说此时HIF-1似乎并没有发挥主要作用,而HIF-2能够提供及时的代偿,但是过度的代偿会诱发血液的高凝状态和高山病。而对于长期居住在高海拔的人群中,经过自然选择,其HIF-2α的基因可能经过了改造,从而凸显或者激发出了HIF-1α的作用,使其能够适应高原生活。
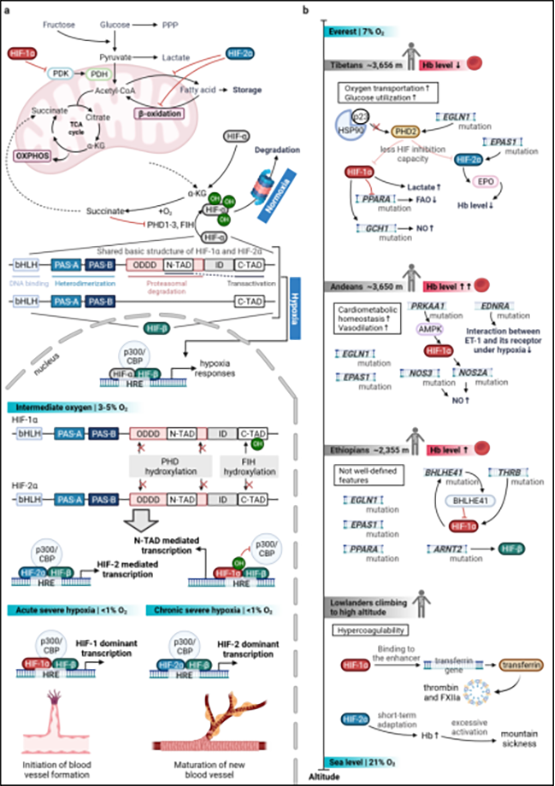
广义上的“HIFs转换”
该文关注了微观上通过后天获得的表观遗传机制和宏观上器官/系统间的交互作用。 缺氧通过一系列表观遗传修饰方式影响心血管疾病的发生和进展,其中包括组蛋白和非组蛋白蛋白质的翻译后修饰、DNA甲基化,以及非编码RNA的调控等(图2)。组蛋白的翻译后修饰涉及心血管疾病的各个方面,包括在动脉粥样硬化和肺动脉高压中内皮细胞对缺氧信号的响应。近期,乳酸化,一种新兴的修饰方式因其在基因转录调控中的关键作用备受关注。有趣的是,在心肌梗死中,乳酸化被认为与心肌纤维化和心脏功能损害有关。此外,乳酸化介导的巨噬细胞极化在炎症性疾病领域也起着关键作用。就 PAH 而言,缺氧诱导的糖酵解转变和乳酸化修饰可能促进缺氧性肺血管重塑(HPVR)。此外,BMPR2 启动子区域的去甲基化可显著改善肺血管和右心室重塑,降低右室收缩压( RVSP)和 平均肺动脉压(mPAP)。气管内输送腺相关病毒封装的 "有益基因 "是一种很有前景的治疗方法。值得注意的是,心血管疾病与 DNA 甲基化以及非编码 RNA 的转录后调控机制之间存在着密切的关系。

心血管疾病缺氧信号的表观遗传调控
地球从早期的厌氧环境到后期光合作用所构建的有氧环境,以及有氧环境所支持的高级生命(包括智人)的发展,这决定了氧气浓度与生物进化及自然节律息息相关(图3)。而昼夜节律和冬眠属于最广泛的两种自然节律,是人或动物对环境应激下的生存策略以及相应的资源利用方式,他们都与缺氧息息相关。目前的研究更多的是强调昼夜节律的改变对HIFs在体内表达幅度的改变。在心血管疾病的病理进程中,与昼夜节律相关的疾病研究得最多的是缺血再灌注损伤。昼夜节律相关分子(如PER2)可以维持HIFs在一定的振幅内波动,这有助于心脏抵抗急性缺血损伤。而心脏中内皮细胞的PER2的失能,将导致其无法在缺氧缺血时有效调用糖酵解、调节线粒体呼吸的平衡以及维持内皮屏障功能。而同样的,长期慢性缺氧,也会破坏昼夜节律分子的作用。除了昼夜节律,另一个与睡眠相关的大自然中常见的生物节律就是冬眠。进一步探究HIFs在“冬眠”中的具体作用以谋求在恒温的哺乳动物中有所转化,例如在急性的心血管事件中使得相应的器官、组织和细胞处于一种能够维持功能的低代谢的“冬眠”状态以休养生息、提供修复和治疗的窗口。其中,HIFs诱导的代谢转向脂肪酸氧化在维持基本代谢并清除多余的ROS等有害物质的过程中起了重要的作用。同时,探究生物体如何在长时间的静止状态下不产生并发症(如压疮、血栓等)对于临床有巨大意义。进一步地,探究生物体如何以“冬眠”的形式用较低的能耗维持机体基本运转和稳态,有助于帮助实现“人类休眠技术”以对抗恶劣环境或是长时间的星际航行。
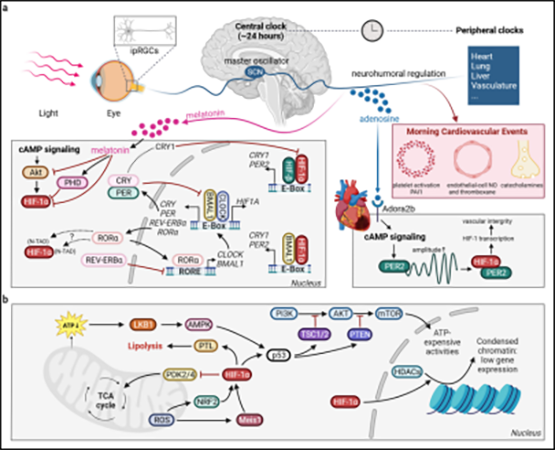
心血管疾病中与HIFs相关的自然节律
缺氧通路在机体中系统性的相互作用可以是通过遍布全身的心血管系统中的组织成分所引起的,如血液(血红蛋白)和脂肪(管周脂肪)等,或者也可以是因为系统性的衰老所导致的心血管系统中多器官的逐渐失能。这种缺氧引起的器官或组织间的相互作用主要是通过神经体液通路实现的,即往往是某一处的器官组织在受到刺激后(如缺血缺氧),释放相应的分泌因子至其周围环境中再通过体液循环至作用的靶器官模拟刺激,构建了相应的作用,这种响应方式一般较慢。更快的相应方式是局部刺激兴奋了相应部位的感受器和传入神经,通过反射弧进行效应器官的作用。这两种方式是可以(并在大多数情况下)是相辅相成共同作用的。其中有代表性的当属HIFs在乳酸穿梭中发挥的作用(图4)。在心脏或其他组织损伤修复的过程中,由乳酸穿梭所诱发,受损区域出现了新生的薄壁毛细血管、成纤维细胞并伴有炎症浸润的状态。这种状态有点类似于涉及表皮或上皮组织损伤修复所形成的“肉芽组织”。其形成和转归都有HIFs的参与。而平衡其时走向再生修复还是纤维化、失能的结局的关键因素仍然有待探究。但从现有的证据而言,早期的干预是尤为重要的。单羧酸转运蛋白1(MCT1)是细胞摄取乳酸并诱发上述进程的起点。根据人类蛋白质图谱,MCT1 在内皮细胞、心肌细胞和成纤维细胞中表达。虽然心肌细胞的MCT1水平最高,但内皮细胞中的MCT1表达水平比成纤维细胞高两倍。而高MCT1表达丰度的细胞最有可能首先从循环中摄取乳酸。从MCT1的表达丰度来看,心脏首先回倾向于自身修复(作用于心肌)和与之相辅相成的血管新生(作用于内皮细胞)。而在疾病发展的后期,Snail-TGFβ所导致的内皮间质转化(EndoMT)将起主导作用。因为,根据人类蛋白质图谱,Snail1在心脏内皮细胞中的表达水平显着高于其他心脏细胞类型,包括心脏成纤维细胞和心肌细胞。高Snail表达丰度的心脏内皮细胞将主导器官纤维化和功能失调的进程。
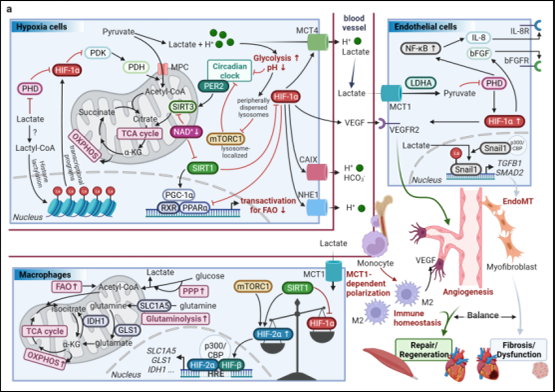
HIF与乳酸穿梭
在药物研发领域,根据SIRT1抑制HIF-1α并激活HIF-2α的特点,SGLT2抑制剂以及resveratol等SIRT1激活剂,以及选择性的PHD抑制剂(激活HIF-2α)(如Cobalt,Roxadustat等)正在被不断探索并用于慢性心血管及肾脏疾病的治疗。总的来说,目前应对时空特异性的"HIFs switch的治疗策略主流之一是:在急性期,维持有效的HIF-1α的激活;在慢性期,保证HIF-2α为主导的效能,与此同时适当的维持HIF-1α的活跃度(图5)。相对应的,目前心血管领域新兴的GLP-1RA、SGLT2抑制剂和PCSK9抑制剂等药物在作用机制上都与HIF通路相关。

心血管疾病中靶向缺氧信号通路的药物
对于HIF相关靶向治疗从基础研究到临床应用的漫漫征途,医生和研发者需要建立深刻的理解,包括HIF相关机制、药物研发历程以及相关治疗方法的发展历史,这将为后续的创新实践提供坚实基础。在临床工作中,需要进行缺氧及相关信号感知详尽的调查研究,识别HIF存在的问题和痛点,将临床医学与基础研究、材料科学、工程应用和信息科学有机结合,同时注重疾病的时空特异性和整体性,从宏观和微观的角度通盘考虑。基于“From the Doctors, By the Engineers, For the Patients”的原则和理念,HIFs相关治疗在心血管医学领域将迎来更多实质性的进展。
论文链接:https://www.nature.com/articles/s41392-023-01652-9
遵义医科大学附属医院党委宣传部
审核:勾强
编辑:肖毅
修改:张洁